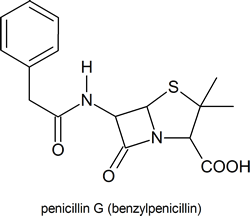21.7: Chemie der Amide
Studienhinweise
Da das Kapitel, das sich mit Aminosäuren und Proteinen beschäftigt, fakultativ ist, ist es möglich, diesen Kurs abzuschließen, ohne diese Verbindungen im Detail zu studieren. Aufgrund ihrer Bedeutung in biologischen Systemen ist es jedoch für alle Studenten, die diesen Kurs abschließen, unerlässlich, einige Kenntnisse über ihre Struktur und Eigenschaften zu haben.
Wenn wir über Aminosäuren sprechen, beziehen wir uns im Allgemeinen auf α-Aminosäuren, d.h. auf Verbindungen, bei denen eine Amino- (NH2) und eine Carboxylgruppe an dasselbe Kohlenstoffatom gebunden sind:
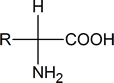
Beachten Sie, dass solche Verbindungen ein chirales Kohlenstoffatom enthalten (außer wenn R = H). Proteine können als aus Aminosäureresten bestehend betrachtet werden, die durch Amid- (oder Peptid-) Bindungen verbunden sind. Diese Peptidbindungen bestehen aus genau den gleichen Struktureinheiten, die wir in sekundären Amiden finden
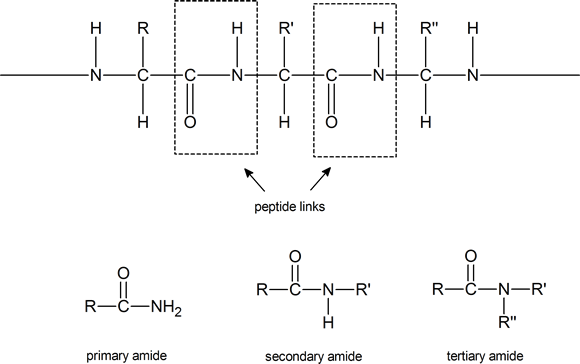
Hinweis: Obwohl hier die Begriffe sekundäres Amid und tertiäres Amid verwendet wurden, stimmt diese Verwendung nicht mit den Empfehlungen der IUPAC überein. Laut IUPAC sollte das oben gezeigte sekundäre Amid als N-substituiertes primäres Amid und das tertiäre Amid als N, N-disubstituiertes primäres Amid bezeichnet werden. Die IUPAC behält den Begriff sekundäres Amid für Verbindungen des Typs
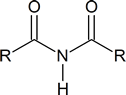
Aufgrund des Vorhandenseins der Amidbindung in Proteinen,
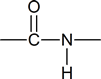
können wir erwarten, dass die Eigenschaften dieser Verbindungen denen der sekundären Amide ähneln.
Ein Lactam ist ein zyklisches Amid, genauso wie ein Lacton ein zyklischer Ester ist:
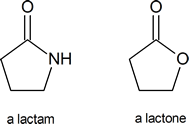
Zu den wichtigsten Molekülen, die Lactamringe enthalten, gehören die Penicilline: