Biologie pratique
Pratique en classe ou démonstration
Le peroxyde d’hydrogène (H2O2) est un sous-produit de la respiration et est fabriqué dans toutes les cellules vivantes. Le peroxyde d’hydrogène est nocif et doit être éliminé dès qu’il est produit dans la cellule. Les cellules fabriquent l’enzyme catalase pour éliminer le peroxyde d’hydrogène.
Cette enquête examine le taux de production d’oxygène par la catalase dans la purée de pommes de terre lorsque la concentration de peroxyde d’hydrogène varie. L’oxygène produit en 30 secondes est recueilli au-dessus de l’eau. Ensuite, la vitesse de réaction est calculée.
Organisation de la leçon
Vous pourriez mener cette enquête sous forme de démonstration à deux concentrations différentes, ou avec des groupes d’élèves travaillant chacun avec une concentration différente de peroxyde d’hydrogène. Les élèves individuels peuvent ensuite avoir le temps de recueillir des données répétées. Des groupes de trois personnes peuvent collecter les résultats pour 5 concentrations différentes et alterner les rôles de manipulateur d’appareils, de lecteur de résultats et de scribe. Le rassemblement et la comparaison des résultats de la classe permettent aux élèves de rechercher les données anormales et incohérentes.
Appareillage et produits chimiques
Pour chaque groupe d’élèves :
Une auge pneumatique/un bol en plastique/un accès à un évier d’eau approprié
Flacon conique, 100 cm3, 2
Seringue (2 cm3) pour s’adapter au deuxième trou de la bonde en caoutchouc, 1
Mesure, 100 cm3, 1
Eprouvette graduée, 50 cm3, 1
Support de pince, bossage et pince, 2
Horloge/chronomètre
Pour la classe – mise en place par le technicien/le professeur :
Peroxyde d’hydrogène, gamme de concentrations, 10 vol, 15 vol, 20 vol, 25 vol et 30 vol, 2 cm3 par groupe de chaque concentration (Note 1)
Purée de pomme de terre, fraîche, dans un bécher avec une seringue pour mesurer au moins 20 cm3, 20 cm3 par groupe par concentration de peroxyde étudiée (Note 2)
Bonde en caoutchouc, 2 trous, pour s’adapter aux flacons coniques de 100 cm3 – tube de refoulement dans un trou (relié à un tube en caoutchouc de 50 cm)
Santé & Notes de sécurité et techniques
Porter des lunettes de protection et couvrir les vêtements lors de la manipulation du peroxyde d’hydrogène.
Laver immédiatement les éclaboussures de purée de pommes de terre ou de peroxyde sur la peau.
Soyez attentif à la pression qui s’accumule si les vaisseaux de réaction se bloquent.
Faites attention en insérant la bonde dans la fiole conique – elle doit être bien ajustée, donc poussez et tournez la bonde avec précaution.
1 Peroxyde d’hydrogène : (Voir la carte des risques du CLEAPSS) Les solutions de moins de 18 vol sont à DANGER FAIBLE. Les solutions à des concentrations de 18-28 vol sont IRRITANTES. Faire attention en retirant le bouchon de la bouteille de réactif, car une pression de gaz peut s’être accumulée à l’intérieur. Diluer immédiatement avant utilisation et mettre dans une bouteille brune propre, car la dilution dilue également l’inhibiteur de décomposition. Conservez les bouteilles brunes car le peroxyde d’hydrogène se dégrade plus rapidement à la lumière. Jetez toute solution non utilisée. Ne remettez pas la solution dans les bouteilles de stock, car les contaminants peuvent provoquer la décomposition et la bouteille de stock peut exploser après un certain temps.
2 La purée de pommes de terre peut irriter la peau de certaines personnes. Faites-en une nouvelle pour chaque leçon, car l’activité de la catalase diminue sensiblement au bout de 2/3 heures. Vous devrez peut-être ajouter de l’eau pour la rendre moins visqueuse et plus facile à utiliser. Les disques de pomme de terre réagissent trop lentement.
3 Si les bulles du tube en caoutchouc sont trop grosses, insérez une pipette en verre ou un tube en verre dans l’extrémité du tube en caoutchouc.
Procédure
SÉCURITÉ : Porter des lunettes de protection et protéger les vêtements du peroxyde d’hydrogène. Rincez le plus rapidement possible les éclaboussures de peroxyde et de purée de pommes de terre sur la peau.
Préparation
a Préparez juste assez de peroxyde d’hydrogène dilué juste avant la leçon. Disposez-le dans des bouteilles brunes (note 1).
b Préparez de la purée de pommes de terre fraîche pour chaque leçon (note 2).
c Préparez des bondes à 2 trous comme décrit dans la liste des appareils et dans le schéma.
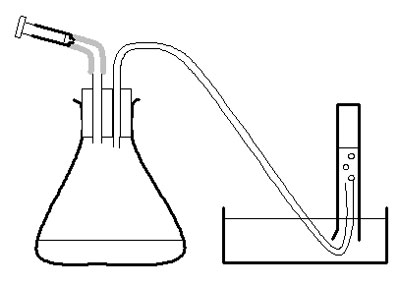
Investigation
d Utilisez la grande seringue pour mesurer 20 cm3 de purée de pommes de terre dans la fiole conique.
e Placez fermement la bonde dans le flacon – tournez et poussez soigneusement.
f Remplissez à moitié l’auge, le bol ou l’évier avec de l’eau.
g Remplissez l’éprouvette graduée de 50 cm3 avec de l’eau. Inversez-le au-dessus de l’auge d’eau, avec l’extrémité ouverte sous la surface de l’eau dans le bol, et avec l’extrémité du tube en caoutchouc dans l’éprouvette graduée. Fixez-le en place.
h Mesurez 2 cm3 de peroxyde d’hydrogène dans la seringue de 2 cm3. Mettez la seringue en place dans la bonde du flacon, mais ne poussez pas le piston tout de suite.
i Vérifiez que le tube en caoutchouc est bien dans le cylindre de mesure. Poussez le piston de la seringue et démarrez immédiatement le chronomètre.
j Après 30 secondes, notez le volume d’oxygène dans l’éprouvette graduée dans un tableau de résultats approprié. (Note 3.)
k Videz et rincez la fiole conique. Mesurez-y un autre 20 cm3 de purée de pommes de terre. Remontez l’appareil, remplissez à nouveau l’éprouvette graduée, et répétez de g à j avec une autre concentration de peroxyde d’hydrogène. Utilisez un cylindre de mesure de 100 cm3 pour les concentrations de peroxyde d’hydrogène supérieures à 20 vol.
l Calculez le taux de production d’oxygène en cm3/s.
m Tracez un graphique du taux de production d’oxygène en fonction de la concentration de peroxyde d’hydrogène.
Notes pédagogiques
Notez les unités de mesure de la concentration de peroxyde d’hydrogène – ce ne sont pas des unités SI. Le peroxyde d’hydrogène de 10 vol produira 10 cm3 d’oxygène à partir de chaque cm3 qui se décompose.(Note 1.)
Dans cette procédure, 2 cm3 de peroxyde d’hydrogène de 10 vol libéreront 20 cm3 d’oxygène si la réaction va jusqu’à son terme. On ajoute à chaque fois 2 cm3 de liquide dans le ballon. Ainsi, si l’appareil ne présente aucune fuite, 22 cm3 d’eau devraient être déplacés dans le cylindre de mesure avec 10 vol de peroxyde d’hydrogène. L’oxygène est soluble dans l’eau, mais ne se dissout que lentement dans l’eau aux températures ambiantes normales.
Utilisez ces informations pour vérifier le montage pratique. Les valeurs inférieures à 22 cm3 montrent que l’oxygène s’est échappé, ou que le peroxyde d’hydrogène n’a pas complètement réagi, ou que la concentration de peroxyde d’hydrogène n’est pas celle attendue. Demandez aux élèves d’expliquer comment des valeurs supérieures à 22 cm3 pourraient se produire.
Une erreur de ± 0,05 cm3 dans la mesure de 30 vol de peroxyde d’hydrogène pourrait faire une erreur de ± 1,5 cm3 dans la production d’oxygène.
Le foie contient également de la catalase, mais la manipulation des abats est plus controversée avec les élèves et introduit un plus grand risque d’hygiène. De plus, la réaction est si vigoureuse que les bulles du mélange peuvent entraîner des morceaux de foie dans le tube de livraison.
Si recueillir le gaz sur l’eau est compliqué, et que vous avez accès à une seringue à gaz de 100 cm3, vous pourriez recueillir le gaz dans celle-ci à la place. Veillez à bien serrer la seringue à gaz, mais avec précaution.
La réaction est exothermique. Les élèves peuvent remarquer la chaleur s’ils mettent leurs mains sur la fiole conique. Comment cela affectera-t-il les résultats ?
Santé et sécurité vérifiées, septembre 2008
Téléchargements
Téléchargez la fiche de l’élève ![]() Enquêter sur une réaction contrôlée par une enzyme : catalase et concentration de peroxyde d’hydrogène (67 Ko) avec questions et réponses
Enquêter sur une réaction contrôlée par une enzyme : catalase et concentration de peroxyde d’hydrogène (67 Ko) avec questions et réponses
Liens Web
.