JOP. Journal of the Pancreas
Keywords
Adenocarcinoma, Mucinoso; Associazione; Carcinoma, Intraduttale, Non Infiltrante; Neoplasie del pancreas
INTRODUZIONE
Il carcinoma colloide del pancreas, noto anche come carcinoma solido mucinoso o gelatinoso, è un tumore che ha origine dai dotti pancreatici, ed è stato recentemente riconosciuto come entità distinta. Rappresenta solo circa l’1-3% di tutti i carcinomi pancreatici. La sua principale caratteristica morfologica è la presenza di pozze ben circoscritte di materiale mucinoso, contenenti cellule epiteliali staccate che galleggiano nella mucina.
Il carcinoma colloide pancreatico è considerato un sottotipo distinto di neoplasia mucinosa papillare intraduttale (IPMN); questo fatto è importante perché può dettare il trattamento chirurgico. Una diagnosi differenziale tra il carcinoma colloide e l’adenocarcinoma duttale è essenziale, perché le differenze biologiche e molecolari tra questi tipi di tumore inducono un decorso clinico più indolente, un miglior risultato dopo il trattamento chirurgico e una sopravvivenza più lunga del primo.
Questo case report descrive le caratteristiche cliniche di un paziente con un carcinoma colloidale pancreatico localmente invasivo, la gestione chirurgica e l’esito.
Rapporto del caso
Un uomo di 64 anni, con una storia medica passata di pressione alta e diabete di tipo 2 è stato valutato nel nostro ambulatorio a causa dell’anemia. Lamentava anche una lieve dispepsia e dolore lombare negli ultimi 18 mesi. Gli esami del sangue convenzionali hanno mostrato un’anemia microcitica. I marcatori tumorali erano normali, tranne il CA 19-9 203 U/mL (gamma di riferimento: 0-39 U/mL). Una tomografia computerizzata (CT) a contrasto dell’addome ha mostrato una massa disomogenea a bassa densità di 12×7 cm, proveniente dal corpo e dalla coda del pancreas. La massa invadeva la parete gastrica posteriore, la flessura splenica del colon e la milza. L’arteria mesenterica superiore e l’asse celiaco non erano coinvolti; tuttavia, l’arteria splenica è stata amputata alla sua origine (Figura 1a). Il dotto di Wirsung alla testa del pancreas era allargato (Figura 1b), con trombosi della vena splenica, ipertensione portale segmentale e varici esofagee.
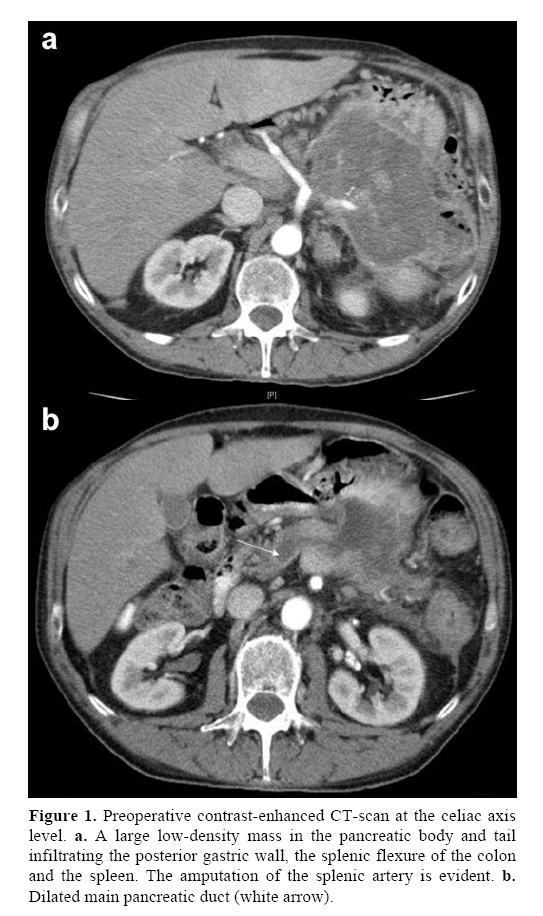
Figura 1. TAC preoperatoria con contrasto a livello dell’asse celiaco. a. Una grande massa a bassa densità nel corpo pancreatico e nella coda che infiltra la parete gastrica posteriore, la flessura splenica del colon e la milza. L’amputazione dell’arteria splenica è evidente. b. Dotto pancreatico principale dilatato (freccia bianca).
La biopsia con ago sottile ha rivelato una neoplasia mucinosa con atipia cellulare che suggerisce una malignità. L’ERCP non poteva essere eseguita a causa di un diverticolo duodenale. Alla laparotomia, è stata osservata una grande massa retroperitoneale che invadeva le strutture circostanti. È stata intrapresa una pancreatectomia distale con splenectomia, gastrectomia totale, resezione di un segmento di colon trasverso e di un pezzo di diaframma. Le biopsie intraoperatorie del margine di dissezione pancreatica hanno mostrato una displasia di alto grado del dotto di Wirsung, quindi è stata eseguita una pancreatectomia di completamento. La ricostruzione è stata fatta con una esofago-giunostomia Roux-Y e una epatico-giunostomia più un’anastomosi colocolica T-T e una chiusura primaria del diaframma sinistro. Il decorso postoperatorio non è stato movimentato e il paziente è stato dimesso il 12° giorno post-operatorio.
L’esame patologico del campione ha dimostrato un carcinoma colloide del pancreas, di 15 cm di diametro, che invadeva localmente la parete gastrica posteriore e il colon trasverso. I margini di resezione retroperitoneale erano privi di invasione. L’esame microscopico ha trovato pozze di mucina con file di cellule epiteliali mucinose che mostravano atipie nucleari, e occasionalmente adottavano un modello ghiandolare (Figura 2). È stato anche osservato un IPMN associato con displasia di alto grado (carcinoma “in situ”) che invadeva l’intero dotto di Wirsung. Non c’era invasione metastatica in nessuno dei linfonodi recuperati. Dopo la valutazione del team multidisciplinare, non è stata indicata alcuna chemioterapia adiuvante.

Figura 2. L’esame istopatologico al microscopio del campione chirurgico ha mostrato le caratteristiche pozze di mucina con file di cellule mucinose epiteliali che mostrano atipia nucleare, e occasionalmente adottano un modello ghiandolare (H&E; ingrandimento originale x10).
A due anni di follow-up, una TAC non ha dimostrato alcuna recidiva del tumore e i marcatori tumorali, compreso il CA 19- 9, erano normali. Il paziente rimane asintomatico e ha una qualità di vita eccellente 24 mesi dopo la procedura.
DISCUSSIONE
Il carcinoma colloide del pancreas è un raro tumore che produce mucosa e deve essere considerato un tipo differenziale di tumore invasivo tra le neoplasie pancreatiche. Si tratta di una neoplasia ben caratterizzata in altri organi, come la mammella, la prostata o il colon, con un comportamento e una prognosi variabili a seconda dei criteri stabiliti per la diagnosi in ciascun organo. Nel pancreas, i carcinomi colloidi mostrano di solito un comportamento clinico indolente, con un modello di crescita lento e una prognosi migliore rispetto agli adenocarcinomi duttali, con un tasso di sopravvivenza a 5 anni vicino al 60% nei casi resecabili. La diagnosi preoperatoria è di grande importanza nel guidare la gestione del paziente: grazie ai progressi nelle tecniche di imaging, i tumori pancreatici possono essere rilevati in fasi precoci e definiti meglio al fine di pianificare un approccio chirurgico accurato.
Il diverso comportamento clinico rivelato dal carcinoma colloide pancreatico può essere in parte legato a due tratti caratteristici di questo tumore: a) l’alterazione della polarità delle cellule tumorali riscontrata all’esame microscopico dove la superficie delle cellule stromali dimostra proprietà secretorie invece della superficie delle cellule duttali; e b) il tipo di mucina secreta dalle cellule tumorali.
La produzione di MUC2 è altamente specifica nel carcinoma colloide mentre MUC1 è secreta nell’adenocarcinoma. Sia MUC1 che MUC2 sembrano avere ruoli importanti nella neoplasia pancreatica. MUC1 sembra essere un marcatore di un fenotipo aggressivo e può facilitare la diffusione vascolare delle cellule tumorali. D’altra parte, MUC2 è comunemente espresso nei tumori con un decorso indolente, come alcuni IPMN e specificamente nei carcinomi colloidi che coinvolgono diversi organi. È stato postulato che la secrezione di MUC2 nello stroma provoca la formazione di uno strato gelatinoso di mucina intorno alle cellule tumorali che limiterebbe la loro diffusione metastatica.
La resezione chirurgica, quando possibile, è il trattamento di scelta in questi tumori. Poiché il carcinoma colloide pancreatico presenta un modello di crescita lenta con invasione locale piuttosto che malattia disseminata, un approccio chirurgico radicale, adattato al modello di invasione locale, può essere giustificato al fine di eseguire una resezione R0. Inoltre, non ci sono dati disponibili sul ruolo della terapia neo-adiuvante per il carcinoma colloide pancreatico localmente avanzato per diminuire il carico tumorale. Tuttavia, come menzionato sopra, la resezione R0 è stata associata ad una sopravvivenza a 5 anni accettabile.
La diagnosi specifica del sottotipo colloide di IPMN può dettare l’estensione della pancreatectomia, poiché lasciare IPMN nel pancreas residuo può mettere il paziente a rischio di recidiva. Una pancreatectomia totale è stata eseguita nel nostro paziente a causa della presenza di noduli sparsi trovati nel dotto di Wirsung residuo che era istologicamente coerente con IPMN con una displasia di alto grado. Il ruolo della terapia adiuvante nei pazienti con carcinoma colloide pancreatico non è stato affrontato in modo specifico. Quando si ottiene una resezione R0, non ci sono prove cliniche che la terapia adiuvante non migliori né la sopravvivenza né i tassi di sopravvivenza libera da malattia.
In sintesi, il carcinoma colloide del pancreas è un raro sottotipo di IPMN che presenta un decorso clinico indolente e un modello di invasione locale. Un approccio chirurgico radicale può essere preferito per ottenere una resezione R0 che può dare una sopravvivenza a 5 anni vicina al 60%. La diagnosi di IPMN invasivo può dettare l’estensione della pancreatectomia. Il ruolo della terapia adiuvante non è stato chiarito.
Conflitto di interessi
Gli autori non hanno alcun potenziale conflitto di interessi
- Andea A, Klimstra D, Cheng J, et al. Colloid carcinoma del pancreas. Curr Diagn Pathol. 2004;10:61-68.
- Adsay N, Pierson C, Sarkar F, et al. Colloid (Mucinous Noncystic) carcinoma del pancreas. Am J Surg Pathol.2001;25:26-42.
- Yopp AC, Katabi N, Janakos M, et al. Carcinoma invasivo derivante da neoplasie mucinose intraduttali papillari del pancreas. Uno studio di controllo abbinato all’adenocarcinoma pancreatico convenzionale. Ann Surg 2011;253:968-974.
- Vo T, Xing Y, Meric-Bernstam F, et al. Esiti a lungo termine in pazienti con carcinomi mucinosi, midollari, tubolari e duttali invasivi dopo lumpectomia. Am J Surg. 2007;194:527-531.
- Waters JA, Schnelldorfer T, Aguilar-Saavedra JR, et al. Survival after resection for invasive intraductal papillary mucinous neoplasmand for pancreatic adenocarcinoma: a multi-institutional comparison according to American Joint Committee on Cancer Stage. J Am CollSurg 2011;213:275-283.
- Tanaka M, Chari S, Adsay V, et al. Linee guida internazionali di consenso per la gestione delle neoplasie mucinose papillari intraduttali e cistiche mucinose del pancreas. Pancreatologia. 2006;6:17-32.
- Levi E, Klimstra DS, Andea A, et al. MUC1 and MUC2 inpancreatic neoplasia. J Clin Pathol. 2004;57:456-462.
- Adsay NV, Merati K, Nassar H, et al. Pathogenesis of colloid (pure mucinous) carcinoma of exocrine organs: coupling of gelformingmucin (MUC2) production with altered cell polarity andabnormal cell-stroma interaction may be the key factor in the morphogenesis and indolent behaviour of colloid carcinoma in thebreast and pancreas. Am J Surg Pathol. 2003;27:571-578.
- Schnelldorfer T, Sarr MG, Nagorney DM, et al. Experience with208 resections for intraductal papillary mucinous neoplasm of the pancreas. Arch Surg. 2008;143:639-646.
- Crippa S, Salvia R, Warshaw AL, et al. Mucinous cysticneoplasm of the pancreas is not an aggressive entity: lessons from163 resected patients. Ann Surg. 2008;247:571-579.
- Turrini O, Waters JA, Schnelldorfer T, et al. Invasive intraductal papillary mucinous neoplasm: predictors of survival and role of adjuvant therapy. HBP (Oxford). 2010;12(7):447-455.