Monosaccharid
Mit wenigen Ausnahmen (z. B. Desoxyribose) haben Monosaccharide diese chemische Formel: (CH2O)x, wobei üblicherweise x ≥ 3 ist. Monosaccharide können nach der Anzahl x der Kohlenstoffatome, die sie enthalten, klassifiziert werden: Triose (3), Tetrose (4), Pentose (5), Hexose (6), Heptose (7) usw.
Glucose, die als Energiequelle und für die Synthese von Stärke, Glykogen und Zellulose verwendet wird, ist eine Hexose. Ribose und Desoxyribose (in RNA bzw. DNA) sind Pentosezucker. Beispiele für Heptosen sind die Ketosen, Mannoheptulose und Sedoheptulose. Monosaccharide mit acht oder mehr Kohlenstoffen werden selten beobachtet, da sie recht instabil sind. In wässrigen Lösungen liegen Monosaccharide als Ringe vor, wenn sie mehr als vier Kohlenstoffe haben.
Linear-kettige MonosaccharideBearbeiten
Einfache Monosaccharide haben ein lineares und unverzweigtes Kohlenstoffgerüst mit einer funktionellen Carbonylgruppe (C=O) und einer Hydroxylgruppe (OH) an jedem der verbleibenden Kohlenstoffatome. Daher kann die Molekülstruktur eines einfachen Monosaccharids als H(CHOH)n(C=O)(CHOH)mH geschrieben werden, wobei n + 1 + m = x; so dass die Elementarformel CxH2xOx lautet.
Nach der Konvention werden die Kohlenstoffatome entlang des Gerüsts von 1 bis x nummeriert, beginnend mit dem Ende, das der C=O-Gruppe am nächsten ist. Monosaccharide sind die einfachsten Einheiten der Kohlenhydrate und die einfachste Form des Zuckers.
Befindet sich das Carbonyl an Position 1 (d. h. n oder m ist Null), beginnt das Molekül mit einer Formylgruppe H(C=O)- und ist technisch gesehen ein Aldehyd. In diesem Fall wird die Verbindung als Aldose bezeichnet. Andernfalls hat das Molekül eine Ketogruppe, ein Carbonyl -(C=O)- zwischen zwei Kohlenstoffen; dann ist es formell ein Keton und wird als Ketose bezeichnet. Ketosen von biologischem Interesse haben meist das Carbonyl an Position 2.
Die verschiedenen oben genannten Klassifizierungen können kombiniert werden, was zu Namen wie „Aldohexose“ und „Ketotriose“ führt.
Eine allgemeinere Nomenklatur für offenkettige Monosaccharide kombiniert eine griechische Vorsilbe zur Angabe der Anzahl der Kohlenstoffe (tri-, tetr-, pent-, hex-, etc.) mit den Suffixen „-ose“ für Aldosen und „-ulose“ für Ketosen. Im letzteren Fall wird dann, wenn das Carbonyl nicht an Position 2 steht, seine Position durch ein numerisches Infix angegeben. So ist zum Beispiel H(C=O)(CHOH)4H eine Pentose, H(CHOH)(C=O)(CHOH)3H eine Pentulose und H(CHOH)2(C=O)(CHOH)2H eine Pent-3-Ulose.
Open-chain stereoisomersEdit
Zwei Monosaccharide mit äquivalenten Molekülgraphen (gleiche Kettenlänge und gleiche Carbonylposition) können dennoch unterschiedliche Stereoisomere sein, deren Moleküle sich in der räumlichen Orientierung unterscheiden. Dies geschieht nur, wenn das Molekül ein stereogenes Zentrum enthält, nämlich ein Kohlenstoffatom, das chiral ist (verbunden mit vier verschiedenen molekularen Unterstrukturen). Diese vier Bindungen können eine von zwei Konfigurationen im Raum haben, die sich durch ihre Händigkeit unterscheiden. In einem einfachen Monosaccharid mit offener Kette ist jedes Kohlenstoffatom chiral, mit Ausnahme des ersten und des letzten Atoms der Kette und (bei Ketosen) des Kohlenstoffatoms mit der Ketogruppe.
Zum Beispiel hat die Triketose H(CHOH)(C=O)(CHOH)H (Glyceron, Dihydroxyaceton) kein stereogenes Zentrum und existiert daher als einzelnes Stereoisomer. Die andere Triose, die Aldose H(C=O)(CHOH)2H (Glyceraldehyd), hat ein chirales Kohlenstoffatom – das zentrale, Nummer 2 – das an die Gruppen -H, -OH, -C(OH)H2 und -(C=O)H gebunden ist. Daher existiert es als zwei Stereoisomere, deren Moleküle spiegelbildlich zueinander sind (wie ein linker und ein rechter Handschuh). Monosaccharide mit vier oder mehr Kohlenstoffen können mehrere chirale Kohlenstoffe enthalten, so dass sie typischerweise mehr als zwei Stereoisomere haben. Die Anzahl der unterschiedlichen Stereoisomere mit demselben Diagramm ist durch 2c begrenzt, wobei c die Gesamtzahl der chiralen Kohlenstoffe ist.
Die Fischer-Projektion ist eine systematische Methode, die Skelettformel eines azyklischen Monosaccharids so zu zeichnen, dass die Händigkeit jedes chiralen Kohlenstoffs gut spezifiziert ist. Jedes Stereoisomer eines einfachen offenkettigen Monosaccharids kann durch die Positionen (rechts oder links) der chiralen Hydroxylgruppen (die Hydroxylgruppen, die an die chiralen Kohlenstoffe gebunden sind) im Fischer-Diagramm identifiziert werden.
Die meisten Stereoisomere sind selbst chiral (verschieden von ihren Spiegelbildern). In der Fischer-Projektion unterscheiden sich zwei spiegelbildliche Isomere dadurch, dass die Positionen aller chiralen Hydroxylgruppen von rechts nach links vertauscht sind. Spiegelbildliche Isomere sind in nicht-chiralen Umgebungen chemisch identisch, haben aber in der Regel sehr unterschiedliche biochemische Eigenschaften und Vorkommen in der Natur.
Während die meisten Stereoisomere paarweise spiegelbildlich angeordnet werden können, gibt es einige nicht-chirale Stereoisomere, die trotz chiraler Zentren identisch mit ihren Spiegelbildern sind. Dies geschieht immer dann, wenn der Molekülgraph symmetrisch ist, wie bei den 3-Ketopentosen H(CHOH)2(CO)(CHOH)2H, und die beiden Hälften spiegelbildlich zueinander sind. In diesem Fall ist die Spiegelung gleichbedeutend mit einer halben Drehung. Aus diesem Grund gibt es nur drei unterschiedliche 3-Ketopentose-Stereoisomere, obwohl das Molekül zwei chirale Kohlenstoffe besitzt.
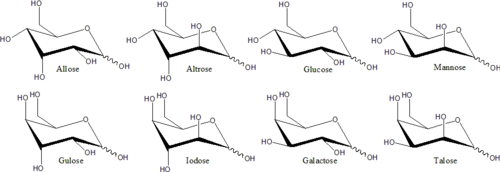
Unterschiedliche Stereoisomere, die keine Spiegelbilder voneinander sind, haben normalerweise unterschiedliche chemische Eigenschaften, auch in nicht-chiralen Umgebungen. Daher kann jedem Spiegelpaar und jedem nicht-chiralen Stereoisomer ein spezifischer Monosaccharid-Name gegeben werden. Zum Beispiel gibt es 16 verschiedene Aldohexose-Stereoisomere, aber der Name „Glucose“ steht für ein bestimmtes Spiegelpaar von Aldohexosen. In der Fischer-Projektion hat eines der beiden Glukose-Isomere das Hydroxyl links an C3 und rechts an C4 und C5, während das andere Isomer das umgekehrte Muster hat. Diese spezifischen Monosaccharidnamen haben konventionelle dreibuchstabige Abkürzungen, wie „Glu“ für Glucose und „Thr“ für Threose.
Generell hat ein Monosaccharid mit n asymmetrischen Kohlenstoffen 2n Stereoisomere. Die Anzahl der Stereoisomere mit offener Kette ist bei einem Aldose-Monosaccharid um eins größer als bei einem Ketose-Monosaccharid gleicher Länge. Jede Ketose hat 2(n-3) Stereoisomere, wobei n > 2 die Anzahl der Kohlenstoffe ist. Jede Aldose hat 2(n-2) Stereoisomere, wobei n > 2 die Anzahl der Kohlenstoffe ist. Diese werden auch als Epimere bezeichnet, die eine unterschiedliche Anordnung von -OH- und -H-Gruppen an den asymmetrischen oder chiralen Kohlenstoffatomen haben (dies gilt nicht für die Kohlenstoffe mit der funktionellen Carbonylgruppe).
Konfiguration von Monosacchariden
Wie viele chirale Moleküle drehen die beiden Stereoisomere des Glycerinaldehyds die Polarisationsrichtung von linear polarisiertem Licht beim Durchgang durch das Molekül allmählich, auch in Lösung. Die beiden Stereoisomere werden je nach Drehrichtung mit den Präfixen D- und L- bezeichnet: D-Glyceraldehyd ist rechtsdrehend (dreht die Polarisationsachse im Uhrzeigersinn), während L-Glyceraldehyd linksdrehend ist (dreht sie gegen den Uhrzeigersinn).

D- und L-Glucose
Die Vorsilben D- und L- werden auch bei anderen Monosacchariden verwendet, um zwei bestimmte Stereoisomere zu unterscheiden, die spiegelbildlich zueinander sind. Dazu betrachtet man den chiralen Kohlenstoff, der am weitesten von der C=O-Gruppe entfernt ist. Seine vier Bindungen müssen sich mit -H, -OH, -C(OH)H und dem Rest des Moleküls verbinden. Wenn das Molekül im Raum so gedreht werden kann, dass die Richtungen dieser vier Gruppen mit denen der analogen Gruppen im C2 des D-Glyceraldehyds übereinstimmen, erhält das Isomer das Präfix D-. Andernfalls erhält es das Präfix L-.
In der Fischer-Projektion geben die Präfixe D- und L- die Konfiguration an dem Kohlenstoffatom an, das das zweite von unten ist: D-, wenn das Hydroxyl auf der rechten Seite steht, und L-, wenn es auf der linken Seite steht.
Beachten Sie, dass die D- und L-Präfixe nicht die Drehrichtung des polarisierten Lichts angeben, die ein kombinierter Effekt der Anordnung an allen chiralen Zentren ist. Die beiden Enantiomere werden das Licht jedoch immer in entgegengesetzte Richtungen drehen, und zwar um den gleichen Betrag. Siehe auch D/L-System.
Zyklisierung von Monosacchariden
Ein Monosaccharid geht oft von der azyklischen (offenkettigen) Form in eine zyklische Form über, und zwar durch eine nukleophile Additionsreaktion zwischen der Carbonylgruppe und einem der Hydroxylgruppen desselben Moleküls. Durch die Reaktion entsteht ein Ring aus Kohlenstoffatomen, der durch ein verbrückendes Sauerstoffatom geschlossen wird. Das resultierende Molekül hat eine Halbacetal- oder Halbiketalgruppe, je nachdem, ob die lineare Form eine Aldose oder eine Ketose war. Die Reaktion lässt sich leicht umkehren, so dass die ursprüngliche offenkettige Form entsteht.
Bei diesen cyclischen Formen hat der Ring meist fünf oder sechs Atome. Diese Formen werden Furanosen bzw. Pyranosen genannt – in Analogie zu Furan und Pyran, den einfachsten Verbindungen mit demselben Kohlenstoff-Sauerstoff-Ring (allerdings fehlen ihnen die Doppelbindungen dieser beiden Moleküle). So kann z. B. die Aldohexose Glucose eine Halbacetalbindung zwischen dem Hydroxyl am Kohlenstoff 1 und dem Sauerstoff am Kohlenstoff 4 bilden, wodurch ein Molekül mit einem 5-gliedrigen Ring entsteht, das Glucofuranose genannt wird. Die gleiche Reaktion kann zwischen den Kohlenstoffen 1 und 5 stattfinden, um ein Molekül mit einem 6-gliedrigen Ring zu bilden, das Glucopyranose genannt wird. Zyklische Formen mit einem siebenatomigen Ring (wie bei Oxepan), die selten vorkommen, werden Heptosen genannt.


Bei vielen Monosacchariden (einschließlich Glucose), überwiegen sowohl im festen Zustand als auch in Lösungen die zyklischen Formen, so dass für die offen- und geschlossenkettigen Isomere meist der gleiche Name verwendet wird. So kann z. B. der Begriff „Glucose“ für Glucofuranose, Glucopyranose, die offenkettige Form oder ein Gemisch der drei Formen stehen.
Durch die Zyklisierung entsteht ein neues stereogenes Zentrum am carbonylhaltigen Kohlenstoff. Die -OH-Gruppe, die den Sauerstoff des Carbonyls ersetzt, kann in zwei verschiedenen Positionen relativ zur Mittelebene des Rings enden. So ergibt jedes offenkettige Monosaccharid zwei zyklische Isomere (Anomere), die mit den Vorsilben α- und β- bezeichnet werden. Das Molekül kann zwischen diesen beiden Formen durch einen als Mutarotation bezeichneten Prozess wechseln, der in einer Umkehrung der ringbildenden Reaktion mit anschließender erneuter Ringbildung besteht.
Haworth-ProjektionBearbeiten
Die stereochemische Struktur eines cyclischen Monosaccharids kann in einer Haworth-Projektion dargestellt werden. In diesem Diagramm hat das α-Isomer für die Pyranoseform einer D-Aldohexose das -OH des anomeren Kohlenstoffs unterhalb der Ebene der Kohlenstoffatome, während das β-Isomer das -OH des anomeren Kohlenstoffs oberhalb der Ebene hat. Pyranosen nehmen typischerweise eine Stuhlkonformation ein, ähnlich der von Cyclohexan. In dieser Konformation hat das α-Isomer das -OH des anomeren Kohlenstoffs in axialer Position, während das β-Isomer das -OH des anomeren Kohlenstoffs in äquatorialer Position hat (bei D-Aldohexosezuckern).
-
α-D-Glucopyranose
-
β-D-Glucopyranose