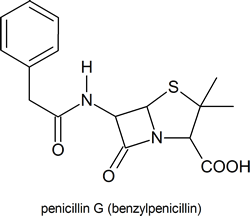21.7: Chemie van amiden
Studienotities
Aangezien het hoofdstuk over aminozuren en eiwitten facultatief is, is het mogelijk deze cursus af te ronden zonder deze verbindingen in detail te bestuderen. Vanwege hun belang in biologische systemen is het echter essentieel dat alle studenten die deze cursus volgen enige kennis hebben van hun structuur en eigenschappen.
Wanneer we het over aminozuren hebben, hebben we het over het algemeen over α-aminozuren; dat wil zeggen, verbindingen waarin een aminogroep (NH2) en een carboxylgroep aan hetzelfde koolstofatoom zijn verbonden:
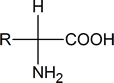
Merk op dat dergelijke verbindingen een chiraal koolstofatoom bevatten (tenzij R = H). Eiwitten kunnen worden beschouwd als bestaande uit aminozuurresiduen die met elkaar verbonden zijn door amide- (of peptide-)verbindingen. Deze peptideverbindingen bestaan uit precies dezelfde structurele eenheden die we in secundaire amiden aantreffen
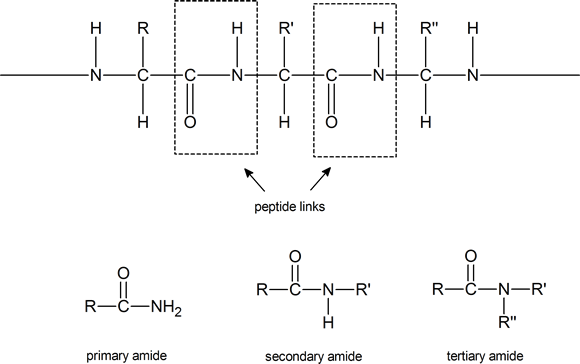
Notitie: Hoewel de termen secundaire amide en tertiaire amide hier zijn gebruikt, is dit gebruik niet in overeenstemming met de IUPAC-aanbevelingen. Volgens de IUPAC moet bovenstaand secundair amide worden aangeduid als een N-gesubstitueerd primair amide, en moet het tertiaire amide worden aangeduid als een N, N-gesubstitueerd primair amide. De IUPAC reserveert de term secundair amide voor verbindingen van het type
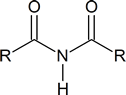
Omdat de amideschakel in eiwitten aanwezig is,
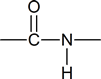
we kunnen verwachten dat de eigenschappen van deze verbindingen lijken op die van secundaire amiden.
Een lactam is een cyclische amide, zoals een lacton een cyclische ester is:
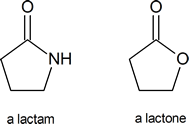
Een van de belangrijkste moleculen die lactam-ringen bevatten zijn de penicillines: