5.1: Isomeren
Optische isomeren
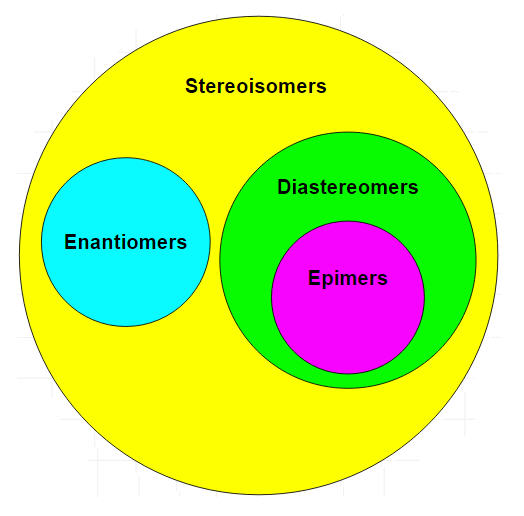
Stereoisomeren die geen geometrische isomeren zijn, worden optische isomeren genoemd. Optische isomeren verschillen in de plaatsing van gesubstitueerde groepen rond een of meer atomen van het molecuul. Zij hebben hun naam te danken aan hun interacties met vlak gepolariseerd licht. Optische isomeren worden aangeduid als enantiomeren of diastereomeren.
Enantiomeren zijn niet-superimpositioneerbare spiegelbeelden. Een veel voorkomend voorbeeld van een paar enantiomeren zijn je handen. Je handen zijn spiegelbeelden van elkaar, maar hoe je je handen ook draait, verdraait of roteert, ze zijn niet superponeerbaar.

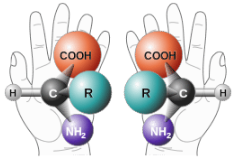
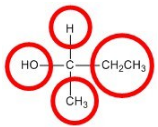
Voorwerpen die niet-superimposabele spiegelbeelden hebben, worden chiraal genoemd. Bij het onderzoeken van een molecuul worden koolstofatomen met vier unieke groepen eraan als chiraal beschouwd. Kijk naar de figuur hieronder om een voorbeeld van een chiraal molecuul te zien. Merk op dat we verder moeten kijken dan het eerste atoom dat aan het centrale koolstofatoom vastzit. De vier cirkels geven de vier unieke groepen aan die aan het centrale koolstofatoom vastzitten, wat chiraal is.
Een ander type optisch isomeer zijn diastereomeren, dat zijn optische isomeren die geen spiegelbeeld zijn. Diastereomeren hebben een verschillende schikking rond een of meer atomen, terwijl sommige atomen dezelfde schikking hebben. Zoals te zien is in de figuur hieronder, is de oriëntatie van de groepen op de eerste en de derde kool verschillend, maar de tweede blijft dezelfde, zodat ze niet hetzelfde molecuul zijn. De ononderbroken wig geeft aan dat een groep uit de pagina/het scherm naar je toe komt en de stippellijn geeft aan dat een groep “achter” de pagina/het scherm van je weggaat.
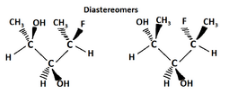
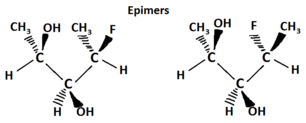
Epimeren zijn een subgroep van diastereomeren die slechts op één plaats verschillen. Alle epimeren zijn diastereomeren, maar niet alle diastereomeren zijn epimeren.