JOP. Journal of the Pancreas
Keywords
Adenocarcinoom, Mucineus; Associatie; Carcinoom, Intraductaal, Niet-infiltrerend; Pancreatic Neoplasms
INLEIDING
Colloïd carcinoom van de pancreas, ook bekend als solide mucineus of gelatineus carcinoom, is een tumor die uitgaat van de pancreaskanalen, en is recentelijk erkend als een aparte entiteit. Het vertegenwoordigt slechts ongeveer 1-3% van alle pancreascarcinomen. Het belangrijkste morfologische kenmerk is de aanwezigheid van goed omlijnde poelen van mucineus materiaal, met daarin losgemaakte epitheelcellen die in het mucine drijven.
Pancreas colloïd carcinoom wordt beschouwd als een apart subtype van intraductaal papillair mucineus neoplasma (IPMN) ; dit feit is belangrijk omdat het de chirurgische behandeling kan dicteren. Een differentiële diagnose tussen colloïd carcinoom en ductaal adenocarcinoom is essentieel, omdat de biologische en moleculaire verschillen tussen deze tumortypes leiden tot een meer indolent klinisch beloop, een beter resultaat na chirurgische behandeling en een langere overlevingskans van de eerste groep.
Dit casusverslag beschrijft de klinische kenmerken van een patiënt met een lokaal-invasief pancreas colloïdcarcinoom, het chirurgisch management en de uitkomst.
CASE REPORT
Een 64-jarige man, met in het verleden een medische voorgeschiedenis van hoge bloeddruk en diabetes type 2, werd in onze polikliniek geëvalueerd vanwege bloedarmoede. Hij klaagde ook over lichte dyspepsie en lage rugpijn gedurende de laatste 18 maanden. Conventionele bloedtesten toonden microcytische anemie. Tumormarkers waren normaal, behalve CA 19-9 203 U/mL (referentiebereik: 0-39 U/mL). Een contrast-verrijkte computertomografie (CT) van de buik toonde een 12×7 cm grote inhomogene massa met lage dichtheid, afkomstig van het lichaam en de staart van de pancreas. De massa drong binnen in de achterste maagwand, de flexuur van de milt van het colon en de milt. De superieure mesenteriale slagader en de as van de coeliacus waren niet betrokken; de miltenslagader werd echter geamputeerd bij de oorsprong (figuur 1a). De Wirsung duct aan de pancreaskop was vergroot (figuur 1b), met splenische veneuze trombose, segmentale portale hypertensie en slokdarmvarices.
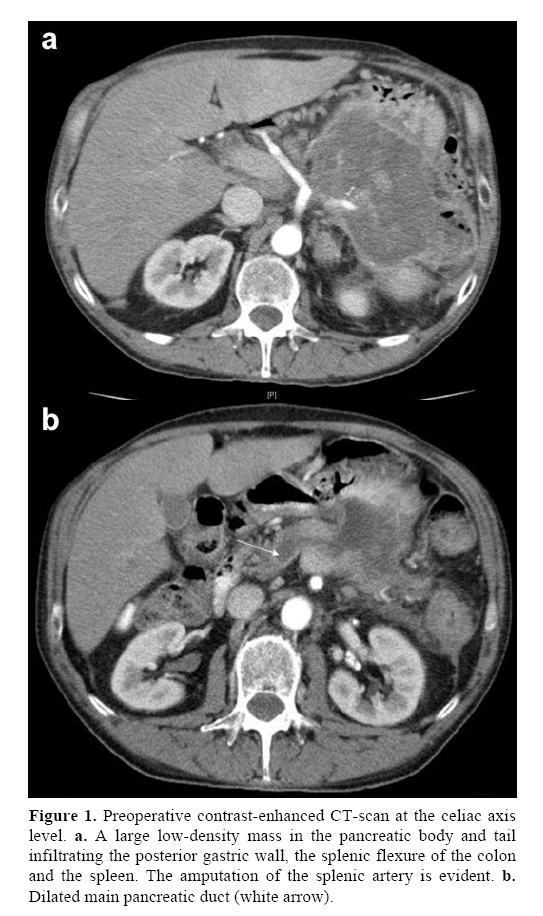
Figuur 1. Preoperatieve CT-scan met contrastversterking ter hoogte van de as van de coeliacus. a. Een grote massa met lage dichtheid in het pancreaslichaam en de pancreasstaart infiltrerend in de achterste maagwand, de flexuur van de milt van het colon en de milt. De amputatie van de miltader is duidelijk. b. Een uitgezette hoofdgang van de pancreas (witte pijl).
Fine-needle aspiratiebiopsie toonde een mucineus neoplasma met cellulaire atypie die op maligniteit wijst. ERCP kon niet worden uitgevoerd vanwege een duodenaal divertikel. Bij de laparotomie werd een grote retroperitoneale massa waargenomen die de omliggende structuren binnendrong. Er werd een distale pancreatectomie uitgevoerd met splenectomie, totale gastrectomie, resectie van een segment van het transversale colon en een patch van het middenrif. Intraoperatieve biopten van de marge van de pancreatische doorsnijding toonden dysplasie van hoge graad van het Wirsung-kanaal, zodat een voltooide pancreatectomie werd uitgevoerd. De reconstructie werd uitgevoerd door een Roux-Y oesofagojejunostomie en hepaticojejunostomie plus een T-T colocolische anastomose en primaire sluiting van het linker diafragma. Het postoperatieve beloop was rustig en de patiënt werd op de 12e postoperatieve dag ontslagen.
Het pathologisch onderzoek van het specimen toonde een colloïd carcinoom van de pancreas aan, 15 cm in diameter, dat lokaal de achterste maagwand en het transverse colon was binnengedrongen. Retroperitoneale resectiemarges waren vrij van invasie. Bij microscopisch onderzoek werden poelen mucine gevonden met rijen epitheliale mucineuze cellen die nucleaire atypie vertoonden, en soms een klierpatroon aannamen (Figuur 2). Geassocieerde IPMN met dysplasie van hoge graad (‘in situ’ carcinoom) die het volledige Wirsung-kanaal binnendrong, werd ook waargenomen. In geen van de opgehaalde lymfeklieren was sprake van metastatische invasie. Na evaluatie door het multidisciplinaire team was geen adjuvante chemotherapie geïndiceerd.

Figuur 2. Microscopisch histopathologisch onderzoek van de chirurgische preparaten toonde de karakteristieke slijmplassen met rijen epitheliale mucineuze cellen die atypie in de kernen vertoonden, en soms een klierpatroon vertoonden (H&E; originele vergroting x10).
Tijdens de follow-up na twee jaar toonde een CT-scan geen tumorrecidief aan, en tumormarkers, waaronder CA 19- 9, waren normaal. De patiënt blijft asymptomatisch en heeft een uitstekende kwaliteit van leven 24 maanden na de procedure.
DISCUSSIE
Colloïd carcinoom van de alvleesklier is een zeldzame slijmvliesproducerende tumor die moet worden beschouwd als een differentieel type invasieve tumor onder de pancreas neoplasma’s . Het is een goed gekarakteriseerd neoplasma in andere organen, zoals borst, prostaat of colon, met variabel gedrag en prognose afhankelijk van de vastgestelde criteria voor diagnose in elk orgaan . In de pancreas vertonen colloïd carcinomen gewoonlijk een indolent klinisch gedrag, met een traag groeipatroon en een betere prognose in vergelijking met ductale adenocarcinomen, met een 5-jarig overlevingspercentage van bijna 60% in resectabele gevallen . De preoperatieve diagnose is van groot belang voor de begeleiding van de patiënt: dankzij de vooruitgang in de beeldvormingstechnieken kunnen alvleeskliertumoren in een vroeg stadium worden opgespoord en beter worden gedefinieerd om een nauwkeurige chirurgische aanpak te plannen .
Het verschillende klinische gedrag dat door het pancreas colloïd carcinoom wordt onthuld kan gedeeltelijk worden gerelateerd aan twee karakteristieke kenmerken van deze tumor: a) veranderde tumor-cel polariteit gevonden in microscopisch onderzoek waar het stromale celoppervlak secretorische eigenschappen vertoont in plaats van ductale cel oppervlak; en b) het type mucine dat door de tumorcellen wordt afgescheiden.
De productie van MUC2 is zeer specifiek in colloïd carcinoom terwijl MUC1 wordt afgescheiden in adenocarcinoom . Zowel MUC1 als MUC2 lijken een belangrijke rol te spelen bij pancreasneoplasie. MUC1 lijkt een marker van een agressief fenotype te zijn en kan de vasculaire verspreiding van tumorcellen vergemakkelijken. Anderzijds komt MUC2 vaak tot expressie in tumoren met een indolent beloop, zoals sommige IPMNs en specifiek in colloïd carcinomen waarbij verschillende organen betrokken zijn. Er is verondersteld dat secretie van MUC2 in het stroma de vorming van een gelatine-achtige laag van mucine rond de tumorcellen teweegbrengt, die hun metastatische verspreiding zou beperken.
Chirurgische resectie, indien mogelijk, is de behandeling van keuze bij deze tumoren . Aangezien pancreas colloïd carcinoom een traag groeiend patroon vertoont met lokale invasie in plaats van gedissemineerde ziekte, kan een radicale chirurgische aanpak, afgestemd op het patroon van lokale invasie, gerechtvaardigd zijn om een R0 resectie uit te voeren. Bovendien zijn er geen gegevens beschikbaar over de rol van neoadjuvante therapie voor lokaal gevorderd pancreas colloïd carcinoom om de tumorlast te verminderen. Zoals hierboven vermeld, is R0 resectie echter geassocieerd met een aanvaardbare 5-jaars overleving.
De specifieke diagnose van het colloïde subtype van IPMN kan de uitbreiding van de pancreatectomie dicteren, aangezien het achterlaten van IPMN in het pancreasrestant de patiënt aan risico op recidief kan blootstellen . Bij onze patiënt werd een totale pancreatectomie uitgevoerd vanwege de aanwezigheid van verspreide knobbeltjes in het Wirsung-kanaal dat histologisch consistent was met IPMN met een hooggradige dysplasie. De rol van adjuvante therapie bij patiënten met pancreas colloïd carcinoom is niet specifiek behandeld. Wanneer een R0 resectie is bereikt, is er geen klinisch bewijs dat adjuvante therapie noch de overleving noch de ziektevrije overleving verbetert.
Samenvattend, colloïd carcinoom van de pancreas is een zeldzaam subtype van IPMN dat een indolent klinisch beloop en een lokaal invasiepatroon vertoont. Een radicale chirurgische benadering kan de voorkeur hebben om een R0-resectie te bereiken die een 5-jaars overleving van bijna 60% kan opleveren. De diagnose van invasieve IPMN kan de uitbreiding van de pancreatectomie dicteren. De rol van adjuvante therapie is niet opgehelderd.
Conflict of interest
De auteurs hebben geen potentieel belangenconflict
- Andea A, Klimstra D, Cheng J, et al. Colloïdcarcinoom van de pancreas. Curr Diagn Pathol. 2004;10:61-68.
- Adsay N, Pierson C, Sarkar F, et al. Colloid (Mucineous Noncystic) carcinoma of the pancreas. Am J Surg Pathol.2001;25:26-42.
- Yopp AC, Katabi N, Janakos M, et al. Invasive Carcinoma Arising in Intraductal Papillary Mucinous Neoplasms of the pancreas. A matched control study with conventional pancreaticductal adenocacinoma. Ann Surg 2011;253:968-974.
- Vo T, Xing Y, Meric-Bernstam F, et al. Long-term outcomes in Patients with mucinous, medullary, tubular, and invasive ductal carcinomas after lumpectomy. Am J Surg. 2007;194:527-531.
- Waters JA, Schnelldorfer T, Aguilar-Saavedra JR, et al. Survival after resection for invasive intraductal papillary mucinous neoplasmand for pancreatic adenocarcinoma: a multi-institutional comparison according to American Joint Committee on Cancer Stage. J Am CollSurg 2011;213:275-283.
- Tanaka M, Chari S, Adsay V, et al. International consensus guidelines for management of intraductal papillary mucinousneoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology. 2006;6:17-32.
- Levi E, Klimstra DS, Andea A, et al. MUC1 and MUC2 inpancreatic neoplasia. J Clin Pathol. 2004;57:456-462.
- Adsay NV, Merati K, Nassar H, et al. Pathogenesis of colloid (pure mucinous) carcinoma of exocrine organs: coupling of gelformingmucin (MUC2) production with altered cell polarity andabnormal cell-stroma interaction may be the key factor in the morphogenesis and indolent behaviour of colloid carcinoma in thebreast and pancreas. Am J Surg Pathol. 2003;27:571-578.
- Schnelldorfer T, Sarr MG, Nagorney DM, et al. Experience with208 resections for intraductal papillary mucinous neoplasm of the pancreas. Arch Surg. 2008;143:639-646.
- Crippa S, Salvia R, Warshaw AL, et al. Mucineus cysteus neoplasma van de pancreas is geen agressieve entiteit: lessen uit163 geresecteerde patiënten. Ann Surg. 2008;247:571-579.
- Turrini O, Waters JA, Schnelldorfer T, et al. Invasive intraductal papillary mucinous neoplasm: predictors of survival and role of adjuvant therapy. HBP (Oxford). 2010;12(7):447-455.