É Glaucoma ou uma Neuropatia Óptica?
Tradicionalmente, o glaucoma tem sido visto como uma doença primária do nervo óptico em que o nervo óptico é danificado como resultado de uma alta pressão intra-ocular. Isto faz sentido, uma vez que muitos pacientes com glaucoma aparente presentes na clínica com pressão elevada – e na maioria desses casos, se baixar a PIO, o paciente deixa de progredir.
Glaucoma de tensão normal é também um diagnóstico bastante comum numa clínica de glaucoma, mas este diagnóstico particular diz respeito aos especialistas em glaucoma porque é um dos poucos glaucomas que não se comporta como os outros. Tende a ser mais rapidamente progressivo, difícil de tratar, e pode muitas vezes afectar a visão central antes de os campos periféricos serem afectados. Em particular, a ligação entre pressão elevada e progressão é por vezes inexistente; a maioria dos pacientes com glaucoma irá sair-se bem com uma PIO de 15 mmHg ou inferior, por exemplo, mas estes pacientes não o fazem. Pode tentar resolver o seu problema baixando o que já era uma pressão “normal”, e em muitos casos isso irá funcionar. No entanto, outros pacientes continuarão a mostrar degeneração do nervo óptico.
Earamente na minha carreira decidi especializar-me tanto no glaucoma como na neuro-oftalmologia, concentrando-me na ideia de que o glaucoma é tanto uma neuropatia óptica como uma doença neuro-degenerativa irreversível. Uma questão que surge quando se adopta esta abordagem é a necessidade de identificar os mascaradores de glaucoma de tensão normal. Estes são frequentemente problemas neurodegenerativos, tais como tumores ou traumas no nervo óptico que causam sinais e sintomas semelhantes aos do glaucoma de tensão normal – especificamente, perda da visão central em combinação com defeitos do campo visual. Em alguns casos, é apenas após o tratamento padrão do glaucoma não resolver o problema que se torna evidente que o glaucoma não é a causa da degeneração do nervo óptico.
Trabalho na clínica de neuro-oftalmologia do nosso centro de referência quaternário, muitas vezes trato pacientes enviados para nós por esta razão exacta; os seus sinais e sintomas não conseguiram responder ao tratamento padrão do glaucoma. Como resultado, tive muita experiência com mascaradores de glaucoma de tensão normal. (Também dirijo uma clínica de glaucoma cirúrgico e clínico muito ocupada que não se especializa em problemas neuro-ftalmológicos, onde é igualmente importante identificar estes pacientes de uma forma eficiente.)
Aqui, gostaria de discutir algumas bandeiras vermelhas que poderá encontrar na sua clínica e que o devem levar a considerar a possibilidade de que algo diferente do glaucoma de tensão normal possa estar a causar o problema do seu paciente. Para ajudar a ilustrar estas bandeiras vermelhas, vou partilhar dois casos que consegui no passado recente.
Taking the Road Less Traveled
Um conceito que considero útil ao diagnosticar este tipo de paciente é uma abordagem ao raciocínio clínico apresentada por um colega da Universidade da Pensilvânia. Esta “teoria do processo duplo” sugere que ao examinar um paciente existem dois caminhos, ou sistemas, que podemos seguir. No Sistema 1, os sinais e sintomas do paciente são reconhecíveis e o paciente pode ser tratado de uma forma familiar. Quando decidimos que um paciente se encaixa no Sistema 1, procedemos à nossa análise padrão dos detalhes, e diagnosticamos e tratamos o paciente em conformidade. No caso de pacientes com glaucoma, fazemos as perguntas básicas: O paciente tem emagrecimento na TOC? Mudanças nos campos visuais? TBC? Um historial familiar de glaucoma? As respostas a estas perguntas dizem-nos qual é a melhor forma de gerir o paciente. A gestão de pacientes do Sistema 1 permite-nos ver um grande número de pacientes todos os dias – o que é actualmente necessário para tornar a prática da medicina economicamente viável para qualquer oftalmologista.
Quando a apresentação do paciente não se enquadra no nosso quadro padrão – trabalho de compreensão, mudamos para a abordagem alternativa, Sistema 2. Nestes casos, algo que estamos a encontrar não faz sentido, levando-nos a categorizar este paciente como diferente. Quando estamos no modo Sistema 2, decidimos que seguir o nosso protocolo padrão pode não resolver o problema do paciente. Será necessário mais tempo e esforço para encontrar o tratamento correcto.
Este conceito de dois sistemas é uma premissa simples, mas importante. De facto, capta um aspecto fundamental da forma como funciona a minha clínica de neuro-oftalmologia. Quando recebo uma referência que não se encaixa no quadro padrão do glaucoma, é fácil para mim converter-me a uma linha de ténues Sistema 2. Afinal de contas, estes pacientes têm problemas que escaparam à gestão médica. A questão chave para a maioria dos oftalmologistas, especialmente numa clínica de glaucoma ocupada, é estar alerta para bandeiras vermelhas que indicam que o seu paciente precisa de ser gerido como um paciente do Sistema 2.
Por exemplo, considere um paciente do sexo masculino de 57 anos que veio ter comigo com visão diminuída em ambos os olhos. Quando o vi, o olho direito já tinha sido afectado mais do que o esquerdo; a visão nesse olho estava em declínio há seis meses. Após o início dos sintomas, ele tinha visto dois oftalmologistas. O primeiro era um especialista em retina. A PIO do paciente não estava elevada, pelo que o médico suspeitava que o paciente tinha uma placa embólica; uma espécie de insulto isquémico tinha acontecido à porção inferior da retina, causando a subsequente escavação do nervo óptico. O paciente foi diagnosticado com uma oclusão da artéria retiniana.
No entanto, o paciente continuou a progredir, o que não é típico de uma oclusão da artéria retiniana; normalmente os danos são feitos e não há mais progressão. Dada esta viragem dos acontecimentos, o especialista em retina enviou o doente a um especialista em glaucoma, que o iniciou em latanoprost no olho direito. Apesar do tratamento, a visão do paciente continuou a piorar num período de tempo relativamente curto.
Este é um exemplo de um indivíduo cuja apresentação e história o colocou inicialmente no Sistema 1, até que a falta de resposta ao tratamento tornou claro que algo diferente do glaucoma de tensão normal deve estar a acontecer. Neste momento, ele foi encaminhado para a nossa clínica. Quando vi o paciente, já estava no modo Sistema 2; dois médicos especialistas tinham passado pelas suas caixas de ferramentas de diagnóstico diferencial sem resolver o problema.
br>>>p> 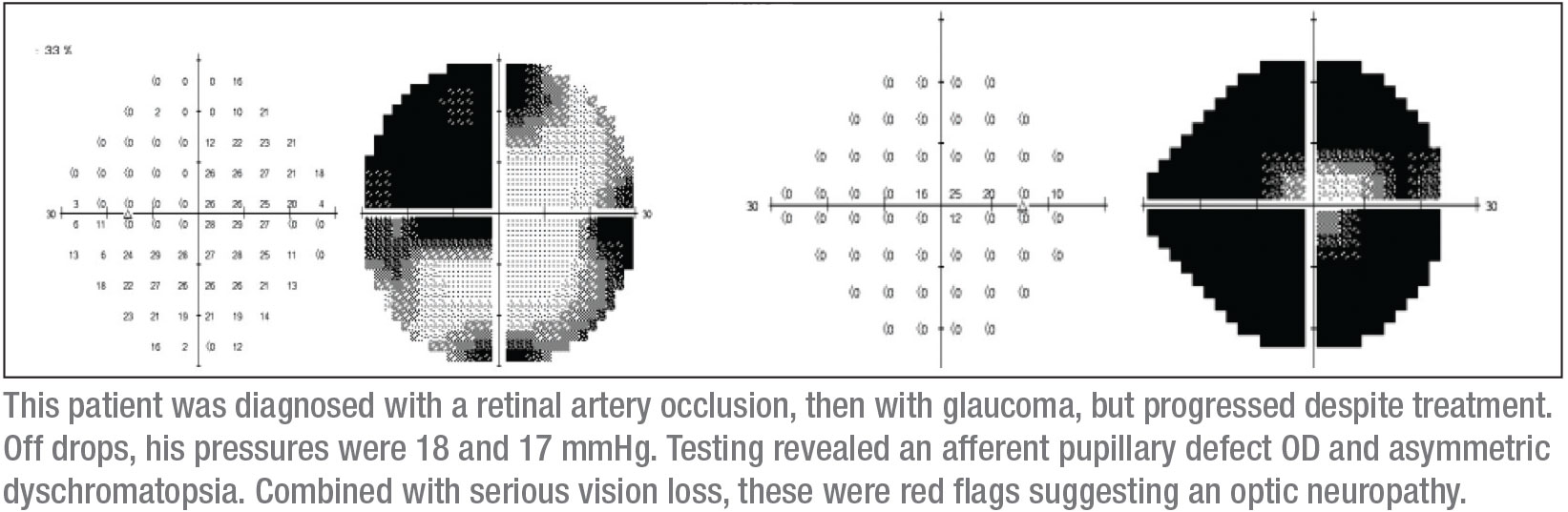 >br>>
>br>>
br>
Examinar o Paciente
p> Na altura em que vi este paciente, a visão no seu olho direito era de contagem de dedos. Normalmente tenho pacientes com tensão normal a parar temporariamente as suas gotas de glaucoma para ver qual é a pressão intra-ocular de base. (Por exemplo, se estiverem sem todas as gotas e a pressão for de 23 mmHg, posso argumentar que a alta pressão está a causar os is-sues, e mantê-los nas suas gotas). Neste caso, o paciente parou a latanoprosta e os seus PIO eram de 18 e 17 mmHg, dentro da gama normal.
O paciente estava geralmente de má saúde; estava com excesso de peso e tinha hipertensão, hiperlipidemia, apneia obstrutiva do sono e diabetes tipo 2. Penso que também é justo dizer que este caso foi complicado pelo facto de este paciente não ser um grande historiador e ser pouco cumpridor. Ele era da Índia continental, e o inglês não era a sua primeira língua, por isso utilizámos um tradutor. Ele não ofereceu muitos detalhes sobre os seus sintomas, dizendo simplesmente: “A minha visão está perdida em ambos os olhos”. Fiz perguntas, tentando obter mais detalhes sobre a natureza da perda da visão; ele apenas disse: “Não sei”.
P>A perda grave da visão foi uma bandeira vermelha porque a maioria dos glaucoma não apresenta inicialmente uma diminuição da visão ou da qualidade visual. O glaucoma precoce é geralmente diagnosticado com um achado de cupping; os pacientes não fazem ideia de que perderam alguma da sua visão periférica. Este paciente nunca admitiu um embaçamento da visão, ou má visão nocturna – o que o pode levar a suspeitar de uma catarata ou de algo reversível. Ele simplesmente disse que tinha tido uma diminuição da sua visão. Isso não me deu muito para continuar, mas ouvir essas palavras de um paciente imediatamente faz-me considerar neuropatia óptica.
Uma série de coisas saltou para fora quando o examinei. Primeiro, ele tinha um defeito pupilar aferente no olho direito. Segundo, a sua visão geral era fraca. Terceiro, ele parecia ter um defeito superotemporal no olho direito. Quarto, o teste de cor revelou uma discromatopsia assimétrica. (Na verdade, a visão no seu olho direito era tão fraca que o teste de cor era inconclusivo nesse olho, mas ele tinha definitivamente discromatopsia no olho esquerdo.)
É atípico que o glaucoma de ângulo aberto seja assimétrico. Acho a assimetria especialmente suspeita quando é extrema – por exemplo, visão deficiente num olho e visão 20/20 no outro. É claro que faço sempre gonioscopia quando encontro doença assimétrica, para procurar quaisquer sinais de recessão angular que possam causar um glaucoma assimétrico. No entanto, não vi qualquer recessão ou dano no ângulo neste paciente.
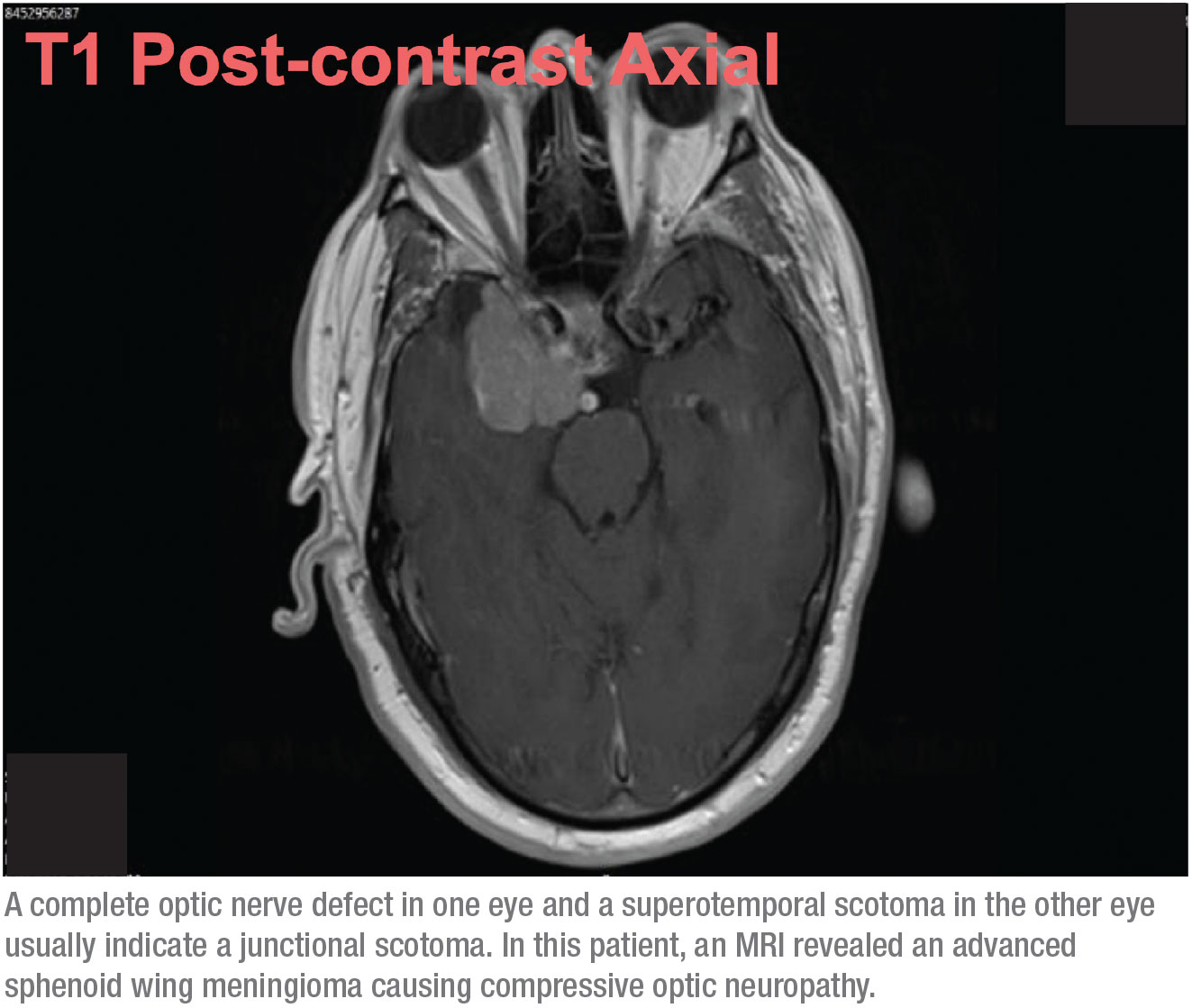 >br>>>>br>>>br>>>p>>p>Minha próxima marca é os campos visuais, que podem ser críticos. Comecei com um teste de campo visual Humphrey, embora soubesse que este paciente poderia não produzir dados de campo visual automatizados fiáveis. De facto, como era de esperar, os parâmetros do campo visual não eram re-confiáveis. No entanto, sugeriram que o olho direito tinha uma pequena ilha central de visão (como esperado), e o olho esquerdo tinha um defeito temporal questionável que não respeitava a linha média vertical. Além disso, obtive um TOC; mostrou um afinamento da retina em ambos os olhos, mas mais no olho direito, o que era consistente com os outros achados clínicos.
>br>>>>br>>>br>>>p>>p>Minha próxima marca é os campos visuais, que podem ser críticos. Comecei com um teste de campo visual Humphrey, embora soubesse que este paciente poderia não produzir dados de campo visual automatizados fiáveis. De facto, como era de esperar, os parâmetros do campo visual não eram re-confiáveis. No entanto, sugeriram que o olho direito tinha uma pequena ilha central de visão (como esperado), e o olho esquerdo tinha um defeito temporal questionável que não respeitava a linha média vertical. Além disso, obtive um TOC; mostrou um afinamento da retina em ambos os olhos, mas mais no olho direito, o que era consistente com os outros achados clínicos.
Senti que ainda precisava de ver campos visuais mais fiáveis. Tenho a vantagem de estar numa instituição académica onde é bastante fácil obter campos visuais-cinéticos de Goldmann que têm um operador presente para explicar e passar tempo com o paciente para desmascarar defeitos visuais de campo fiáveis. Foi um campo visual Goldmann que deu o diagnóstico; mostrou claramente um defeito superotemporal no olho esquerdo, com um defeito quase completo do campo visual no olho direito. (Ver campos, p. 15.) Aquele pequeno círculo no meio do campo visual direito é toda a visão que este doente tinha naquele olho.
Esta combinação de sinais – um defeito do nervo óptico completo num olho, e um escotoma superotemporal no outro olho – traduz-se normalmente num escotoma juncional, um escotoma na junção do nervo óptico e do quiasma, mais conhecido como joelho de von Willebrand. Esta é uma área anatómica de fibras nervosas inferonasais no nervo óptico. Estas fibras estendem o nervo óptico antes de atravessar para o tracto óptico oposto. A lesão quiasmal anterior afecta as fibras nervosas ópticas e as fibras inferonásicas contralaterais localizadas no joelho de von Willebrand. Isto produzirá classicamente uma neuropatia óptica ipsilateral – neste caso manifestando-se como um defeito de campo visual completo e um defeito de campo supratemporal no olho contralateral.
Quando esta possibilidade se apresenta, já não é um problema de glaucoma de tensão normal. Este paciente precisava de uma ressonância magnética. Com base nos campos visuais, sabia que era muito provável que encontrássemos uma massa de crescimento lento no cérebro, como um meningioma, causando uma neuropatia óptica compressiva. De qualquer forma, não esperava que fosse demasiado extensa, por isso fiquei surpreendido quando recebi uma chamada da radiologia depois de a RM ter terminado, dizendo que o meu paciente tinha um turno da linha média, perguntando se deveria ser enviado para neurocirurgia. No início não tinha a certeza se estávamos a falar do mesmo paciente! Mas verificou-se que o tumor estava avançado. (Ver varredura, acima.)
Felizmente, desde que foi submetido à cirurgia, o paciente portou-se bem. Por ser um meningioma, e não um tumor maligno, o cirurgião foi capaz de simplesmente o descomprimir. O paciente teve de facto um pouco de visão no seu olho direito; a visão no seu olho esquerdo não foi quase completamente afectada.
Color Vision e APDs
Além de campos visuais invulgares e exames de OCT, dois outros sinais são altamente sugestivos de problemas neurodegenerativos: défices de visão colorida e defeitos pupilares aferentes.
Não todas as células ganglionares da retina são afectadas igualmente no glaucoma precoce; acredita-se que as células ganglionares da retina koniocelular, que respondem preferencialmente a estímulos azuis/amarelos, sejam afectadas em primeiro lugar. O que isso significa é que a maioria da visão cromática é tipicamente preservada no glaucoma, mesmo em pacientes com glaucoma de tensão normal. Só quando o nervo óptico está morto é que a deficiência de percepção da cor, ou discromatopsia, é óbvia a partir do teste – pelo menos com as placas de cor Ishihara ou pseudo-isocromáticas que tipicamente utilizamos na clínica. (Os testes de visão cromática menos utilizados incluem o teste de visão cromática da City University, o tradicional teste dicotómico D-15, e o teste de visão cromática Farnsworth-Munsell de 100 tonalidades. Todos estes são utilizados para procurar a degeneração da retina, e testam todas as cores ao longo do espectro visual). Ao contrário do glaucoma, a visão a cores não é preservada com doenças neurodegenerativas. Isso torna um défice de visão cromática uma ferramenta útil para diferenciar entre neuropatia óptica e glaucoma.
p>Dois estudos que analisaram o impacto do glaucoma na percepção da cor descobriram que os défices de cor mais comuns em pacientes com glaucoma são os defeitos tridentes, ou azuis/verdes.1,2 Ironicamente, uma limitação das placas pseudo-isocromáticas que usamos na clínica – incluindo o teste de Ishihara – é que não testam os defeitos tridentes. (Na clínica, temos um teste para estimular estas células ganglionares específicas: o teste de campo visual SITA SWAP. Ao contrário de um teste padrão SITA, o SITA SWAP utiliza um fundo azul e uma luz amarela/laranja. Essa combinação de cores pode revelar defeitos indicativos de danos glaucomatosos precoces). No entanto, o teste de cor que normalmente utilizamos na clínica irá detectar os défices causados pelas neuropatias ópticas, porque afectam um conjunto diferente de células ganglionares da retina.
A segunda bandeira vermelha que uma neuropatia óptica pode estar a causar danos no nervo óptico é um defeito pupilar aferente. Isto é uma coisa útil a verificar porque uma DPA raramente é encontrada em glaucoma leve ou precoce.3
E quanto a MRIs?
Uma mulher de 40 anos de idade apresentada na nossa clínica com visão turva num olho – um sintoma que deve sempre levantar suspeitas. Ela tinha ido a um optometrista para óculos três anos antes, onde recebeu um teste padrão de campo visual; o resultado foi anormal. Ela recebeu óculos e foi diagnosticada pelo optometrista como tendo glaucoma no olho direito. Notavelmente, a sua visão escurecida no olho esquerdo não foi ajudada pelos óculos.
O olho direito foi muito subtilmente envolvido. Tinha um defeito minúsculo que inicialmente podia ser interpretado como um artefacto. Isto correspondia a áreas finas superiores na TOC, pelo que fazia sentido concluir que o problema era glaucoma e iniciar a paciente com gotas. (Quando a vi tinha estado a tomar latanoprost e dorzolamida/timolol.) Na altura, não tinha sido testada para um possível APD, nem a sua visão colorida tinha sido avaliada.
Antes de me ver, ela tinha-se perdido para o seguimento durante três anos. Ela voltou com um defeito visual mais impressionante no olho direito que era maior, correspondendo novamente com áreas finas na TOC. Esta aparente progressão fez com que a paciente fosse encaminhada para a minha clínica.
Quando vi a paciente, ela estava basicamente saudável, embora tivesse uma doença mista do tecido conjuntivo. Ela não tinha um historial familiar de glaucoma. Tinha 20/30 OD e 20/25 OS, e depois de ter ficado sem gotas durante algumas semanas, a sua PIO era de 12 mmHg em ambos os olhos. Os seus ângulos eram normais e as suas pupilas eram redondas, mas havia um APD lento no lado direito e uma visão de cor diminuída. Nesta altura, era evidente que algo mais do que glaucoma poderia ser a causa do problema, e a necessidade de uma ressonância magnética era clara.
Isto levanta uma questão muito importante: Se um paciente como este for submetido a uma RM do cérebro ou a uma RM da órbita, com atenção especial para um local específico?
A resposta é esta última – uma RM da órbita. A razão é que os principais sinais radiográficos de um meningioma da bainha do nervo óptico seriam fáceis de perder numa ressonância magnética dedicada ao cérebro. Em contraste, esses sinais podem ser claramente identificados numa ressonância magnética da órbita. Dois desses sinais, por exemplo, são o sinal “doughnut” e o sinal “tram track”. Para ver esses sinais, a órbita tem de ser suprimida com gordura e o exame tem de mostrar fatias finas através da órbita. A única forma de o fazer é se dissermos ao radiologista que queremos uma ressonância magnética orbital (peço frequentemente uma ressonância magnética cerebral e orbital, mas o seguro raramente cobre ambos.)
Quando um meningioma do nervo óptico está presente, o sinal do donut é normalmente claramente visível na ressonância magnética orbital, porque o contraste faz parte desta ressonância. Por exemplo, no exame da página 20, as manchas brancas acima dos nervos ópticos são secções transversais dos vasos sanguíneos, iluminadas por causa do contraste no sangue. Os músculos também são iluminados devido ao fluxo de sangue para essa área, o que é uma melhoria normal. O que normalmente não se ilumina é a bainha do nervo óptico; não se deve ser capaz de ver isso numa imagem como esta. A bainha iluminada visível nesta imagem produz o “sinal de donut” que se pode ver no lado direito da órbita. O diagnóstico é um meningioma da bainha do nervo óptico.
Esta é a principal razão pela qual não gostaria de fazer uma RM ao cérebro de cada paciente com glaucoma de tensão normal; um exame ao cérebro pode muito bem não revelar o diagnóstico correcto. (E, claro, seria uma utilização realmente cara de recursos médicos.)
p> 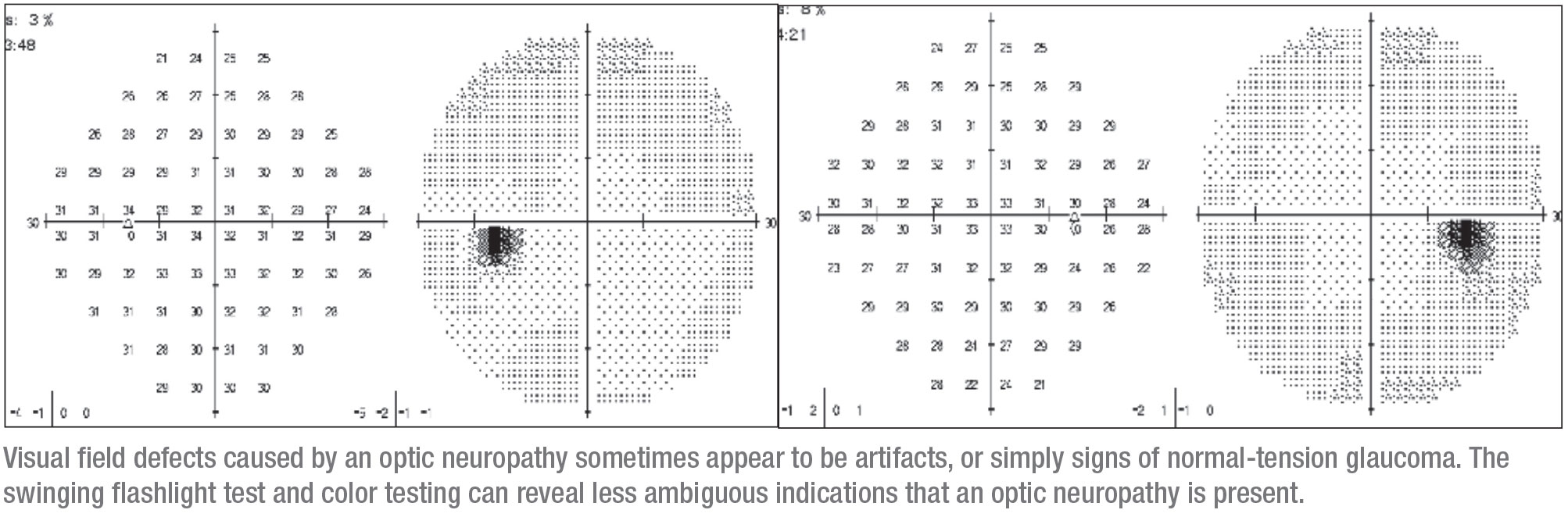 >br>>>/p>>br>>>br>
>br>>>/p>>br>>>br>
Estratégias para o Sucesso
Para ajudar a apanhar bandeiras vermelhas em pacientes que estão de facto a sofrer de uma neuropatia óptica não-lucomatosa na clínica, ou para os deslocar de uma pista do Sistema 1 para uma pista do Sistema 2 o mais cedo possível, mantenha estas estratégias em mente:
– Fazer um teste de cor a cada paciente com glaucoma de tensão normal. Acuidade visual não semelhante, a visão a cores raramente é verificada numa clínica de glaucoma. Provavelmente não é necessário verificar a visão a cores de todos os pacientes com glaucoma, mas os pacientes com glaucoma de tensão normal devem ser testados. Todos os meus técnicos são treinados para verificar a visão a cores, e as placas de Ishihara são mantidas em todas as minhas salas de exame. Além disso, se eu suspeitar durante um exame que algo que não seja glaucoma possa explicar os danos nervosos do paciente, eu próprio farei o teste.
– Dar a todos os pacientes com glaucoma o teste da lanterna de baloiço antes de serem dilatados. A realização do teste demora apenas dois ou três segundos. Claro, isto deve ser sempre feito para novos pacientes, mas também deve ser feito para pacientes que regressam. O ditado de Hickam diz: “Os pacientes podem ter tantos diagnósticos quantos bem entenderem”, e de facto, um paciente que tenho visto durante anos pode desenvolver inesperadamente um tumor, causando um APD, ao mesmo tempo que tem também glaucoma. Um tumor é algo que eu não gostaria de perder.
– Esteja alerta para uma perda de visão constante e sem dor na história. A neuropatia óptica compressiva, como a causada por um tumor, é tipicamente difícil de caracterizar de forma sintomática. No entanto, algumas indicações na história podem ser sugestivas. A neuropatia óptica compressiva não acontece rapidamente, ao contrário dos danos causados pela isquemia, em que se acorda e a visão num olho desaparece. Não dói. Apenas se nota que a visão num olho não é tão viva, nem tão clara, e eventualmente, a visão perde-se completamente. Isto pode acontecer durante um período de oito meses ou mais.
– Uma fraca acuidade visual é uma bandeira vermelha. Outra pista de que pode não estar a lidar com glaucoma é que a maioria dos indivíduos com neuropatia óptica não glaucomatosa têm uma fraca acuidade visual. Em contraste, a maior parte dos tipos de glaucoma não subcutam uma boa acuidade central até às fases finais. (Claro que isso não é verdade em todos os casos de glaucoma de tensão normal; em alguns pacientes, o NTG causa defeitos centrais e paracentrais que podem aproximar-se muito dos 10 graus centrais de vi-sion e afectar a acuidade visual e a fixação por divisão. Mas a má visão central é uma marca distintiva da maioria das neuropatias ópticas não glaucomatosas).
Um estudo feito em 1982 analisou esta questão.4 Os autores avaliaram a acuidade visual e a lesão do nervo óptico após diferentes tipos de insultos ao nervo, incluindo glaucoma, isquemia (de algo como neuropatia óptica isquémica não artérica), compressão, e neuropatia óptica tóxica de drogas como amiodarona ou etambutol. Olharam para a acuidade visual da fase final e correlacionaram-na com o tamanho vertical do copo e a área nervosa, bem como com o número de axónios restantes. O que descobriram foi que a maioria dos doentes com glaucoma tinha acuidade visual entre 20/25 e 20/400, dependendo do estádio da doença. Em média, estes pacientes tinham grandes cabeças nervosas ópticas e tinham mais células ganglionares da retina do que pacientes que tinham sofrido coisas como isquemia ou neuropatia óptica compressiva ou tóxica.
– Verifique a cor da borda nervosa. Nicholas J. Volpe, MD, um co-autor do livro didáctico de neuro-oftalmologia que aprendi como residente e companheiro, e ao qual ainda hoje me refiro, descreveu muitas vezes a palidez ex-tendendo para além da taça até à borda do nervo. Quando qualquer parte da borda do nervo óptico está pálida, isso é um sinal de que o glaucoma pode não ser o único problema, porque na maioria dos glaucomas, por mais avançados que estejam, a borda do nervo óptico permanece rosada. Pode ser extremamente fino por causa da escavação, mas geralmente permanece uma cor saudável até às fases finais da doença. Se vir uma borda que quase parece da mesma cor que a própria taça, isso é um sinal de aviso para aumentar a sua lista de possíveis causas.
– Se um paciente estiver a chegar apenas para uma verificação de pressão ou campo visual, certifique-se de que também são verificados para uma DPA. Uma vez que estes pacientes não estão a ser dilatados, é uma excelente oportunidade para se certificar de que nada neurológico mudou.
– No mínimo, certifique-se de que novos pacientes com glaucoma são verificados quanto a uma DPA e deficiência de visão colorida. Quando chega um novo paciente com glaucoma, antes de fazer o meu exame gonioscópico, olho para os testes de cor que foram feitos pelo meu técnico e verifico se existe uma DPA.
– Se se deparar com uma bandeira vermelha, não hesite em obter uma segunda opinião. Se tiver alguma dúvida sobre se o seu paciente pode ter um problema para além do glaucoma, pedir a um colega pode ser uma opção valiosa. Ouço frequentemente colegas perguntar a minha opinião sobre se os campos de um paciente sugerem um problema neurológico. Obter uma segunda opinião é sempre uma boa ideia.
Ficar atento
A minha experiência tem mostrado que um bom número de pacientes diagnosticados com glaucoma de tensão normal têm na realidade um problema diferente. De qualquer forma, penso que é importante salientar que isto não significa que o médico que fez o diagnóstico de glaucoma de tensão normal tenha feito algo de errado. Pode ser simplesmente que algumas descobertas chave no exame físico – achados que poderiam ter deslocado o paciente para uma pista do Sistema 2 – tenham sido ignoradas, ou que os dados relevantes não tenham sido recolhidos. Nesta situação, a necessidade de uma abordagem do Sistema 2 pode apenas tornar-se aparente quando o paciente não responde ao tratamento padrão do glaucoma.
>br>
>br>>>>br>>p>p>Porque eu também dirijo uma clínica de glaucoma ocupada, compreendo perfeitamente quando os meus colegas me dizem que estão a ver 50 a 80 pacientes por dia e não há maneira de poderem fazer testes de cor em cada paciente. E mesmo com a melhor das intenções, alguns pacientes acabam dilatados antes que o oftalmologista os veja, pelo que nem sempre se pode verificar a existência de um APD. No entanto, vale a pena tentar encaixar estas coisas no fluxo do seu paciente, especialmente quando se trata de um paciente com glaucoma de tensão normal. Mesmo sem testes para deficiências de cor e DPA, olhar cuidadosamente para os campos visuais com os olhos esquerdo e direito lado a lado revelará frequentemente algo que sugere uma patologia neurológica.
Não estou a sugerir que todos os oftalmologistas que tratam glaucoma devam ser capazes de diagnosticar um escotoma juncional ou um meningioma da bainha do nervo óptico. O importante é reconhecer uma bandeira vermelha e perceber que este paciente é diferente dos outros. REVIEW
Dr. Ross é professor assistente, com dupla nomeação nos departamentos de neurologia e oftalmologia do Instituto Scheie Eye e Hospital da Universidade da Pennsylvania. Teve uma bolsa de formação em glaucoma e neuro-oftalmologia.
1. Pacheco-Cutillas M, Edgar DF, Sahraie A. Adquiriu defeitos de visão cromática em glaucoma – a sua detecção e significado clínico. Br J Ophthalmol 1999;83:12:1396-402.
2. Amostra PA, Boynton RM, Weinreb RN. Isolamento da perda de visão cromática no glaucoma primário de ângulo aberto. Am J Ophthalmol 1988;15:106:6:686-91.
3. Rastreio de glaucoma de Charalel RA, Lin HS, Singh K. Glaucoma usando defeito pupilar relativo aferente. J Glaucoma 2014;23:3:169-73.
4. Quigley HA, Addicks EM, Green WR. Lesão do nervo óptico no glaucoma humano. III. Correlação quantitativa da perda de fibras nervosas e defeito do campo visual no glaucoma, neuropatia isquémica, papiledema, e neuropatia tóxica. Arco Ophthalmol 1982;
100:135-146.